P2Y12受体拮抗剂的选择困惑——氯吡格雷还是替格瑞洛?
【2021-05-27】
背景——传统和普识
据《中国心血管健康与疾病报告2019》数据,我国心血管病现患人数3.30亿,其中脑卒中1300万,冠心病1100万,心脑血管病死亡占城乡居民总死亡原因的首位。
心血管疾病主要为冠心病,该病是由于冠状动脉粥样硬化使管腔狭窄或闭塞导致心肌缺血、缺氧或坏死而引发的。急性冠状动脉综合征(ACS)是冠心病的一种类型,包括不稳定型心绞痛、急性ST段抬高性心肌梗死(STEMI)和急性非ST段抬高性心肌梗死(NSTEMI)。
对于ACS患者及经皮冠状动脉介入(PCI)术后的患者来说,阿司匹林联合1种P2Y12受体抑制剂的双联抗血小板治疗(DAPT)是抗栓治疗的基础。目前P2Y12受体拮抗剂临床上主要使用氯吡格雷和替格瑞洛。
氯吡格雷
氯吡格雷为第二代抗血小板聚集药物,主要通过选择性地与血小板表面的二磷酸腺苷(ADP)受体结合从而不可逆地抑制血小板聚集。 对于ACS患者传统强化双联抗血小板为“阿司匹林+氯吡格雷”联合用药。在首次或再次PCI之前应尽快服用氯吡格雷初始负荷量300 mg,后续服用氯吡格雷75mg/d,未置入支架的患者至少28天,支架置入的患者术后均应使用至少12个月。
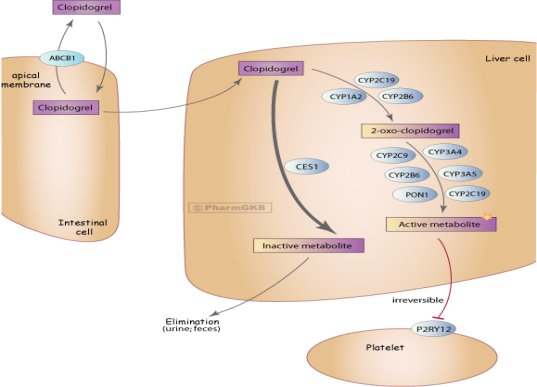
CLARITY-TIMI28研究显示在阿司匹林和溶栓基础治疗上,加用氯吡格雷组STEMI患者主要终点事件相对风险与安慰剂组相比降低36%(P<0.001)。COMMIT-CCS2研究对发病24小时内中国急性心肌梗死患者(93%为STEMI)进行研究,结果显示阿司匹林联合氯吡格雷组较安慰剂组显著降低复合终点的相对风险9%,同时显著降低死亡风险7%,无论患者是否接受溶栓治疗均可获益。对于ACS患者,无论是否接受介入治疗,均可考虑双联抗血小板治疗,疗程12~36个月。
替格瑞洛
替格瑞洛是一种新型的环戊基三唑嘧啶类(CPTP)口服抗血小板药物,为非前体药,无需经肝脏代谢激活即可直接起效,与P2Y12受体可逆性结合。
PLATO研究结果显示,替格瑞洛治疗12个月,在不增加主要出血的情况下,较氯吡格雷进一步显著降低ACS患者的心血管死亡/心肌梗死/脑卒中复合终点事件风险达16%,同时显著降低心血管死亡风险达21%。研究显示,对于STEMI溶栓后转运PCI患者,PCI术前使用替格瑞洛的血小板抑制效果优于氯吡格雷。
基于替格瑞洛治疗给ACS患者带来的获益,国内外的相关指南均推荐,替格瑞洛限制条件下用于ACS患者。在ESC的多部权威指南(2015年ESC NSTE-ACS指南、2017年STEMI指南、2017 DAPT指南)中更是指出,只有在不能接受替格瑞洛治疗的患者中才能使用氯吡格雷,也充分显示了对于替格瑞洛进一步降低死亡率的认可。目前我国STEMI及NSTEMI指南对于替格瑞洛的使用均为ⅠA类推荐。
2016年替格瑞洛专家共识指出,对于STEMI患者,缺血风险中、高危及计划行早期侵入性诊治的NSTE-ACS患者应尽早使用替格瑞洛。除非有明确禁忌,该药应与阿司匹林联用,对于行PCI的ACS患者,默认DAPT的疗程应为12个月;在高出血风险的患者(如PRECISE-DAPT评分≥25分)应考虑6个月的DAPT;在可耐受DAPT且无出血并发症的ACS患者可以考虑超过12个月的治疗。对于高危缺血心肌梗死患者,若耐受DAPT且无出血并发症,可考虑阿司匹林联用替格瑞洛60 mg,每日2次,用于12个月以上延长期治疗,维持36个月(ESC 2017 DAPT指南Ⅱb/ B)。对于行PCI的稳定性冠心病患者,在考虑了缺血风险和出血风险后,可考虑替格瑞洛替代氯吡格雷联合阿司匹林治疗(ESC 2017 DAPT指南Ⅱb/ C)。
目前国内中大型医疗机构ACS的药物干预治疗中,首选替格瑞洛已成共识并形成一定市场规模。
应用——困惑和选择
一、氯吡格雷的困惑
氯吡格雷为传统用药,临床时间较长、经验较多,但确实也存在氯吡格雷抵抗的困惑。氯吡格雷抵抗是指氯吡格雷标准疗法(起始300 mg负荷量,75 mg/d维持量)不能使患者减少或免除缺血性血管事件的发生,并且检测的血小板聚集功能没有被有效抑制。该机制尚不明确,包括内源性、外源性多个因素,内源性包括P2Y12、CYP3A4、糖蛋白Ⅱb/Ⅲa等基因多态性及ADP和其他血小板活化途径等相关因素,外源性包括服药剂量、依从性、药物相互作用及检测方法不一等。目前主要研究热点包括基因多态性、药物剂量、药物相互作用、其他因素(体重指数、胰岛素抵抗)等等。
其中基因多态性方面具有非外源干扰性、检测可行性、预期结果判读性的特点。研究较多的是氯吡格雷的低反应性与其代谢通路上CYP2C9、CYP3A4或CYP3A5、CYP2C19、ABCB1和P2Y12R等基因的多态性有关。目前对于CYP2C19的研究最为清楚。CYP2C19有多个不同位点的等位基因,对氯吡格雷代谢的作用强度不同,其中*1为正常功能等位基因,*2、*3为功能缺失或是降低等位基因。*2、*3在国内人群中分布较多,携带*2和*3 CYP2C19功能缺失等位基因患者与非携带者相比,出现心血管死亡、心肌梗死、支架内血栓的风险显著增加,可以定性预判冠心病易患风险、氯吡格雷抵抗、支架内再狭窄等预期风险评估。所以,临床上有必要进行基因检测,筛出不同类型人群,指导氯吡格雷合理使用。而血小板聚集试验和血栓弹力图等实验室检验是结论性的评估手段,不能达到前瞻和预判分类的目的,不能满足临床精准实操要求。
药物基因组学的迅猛发展为我们提供了关联药物基因检测的可能,并且已经成为指导临床个体化用药、评估严重药物不良反应发生风险的重要工具。国家卫计委2015年发布了《药物代谢酶和药物作用靶点基因检测技术指南(试行)》中,明确指出氯吡格雷的检测位点CYP2C19等位基因。美国FDA已批准了该药物的药物基因组信息,而Pharmgkb(药物基因组学数据库)、CPIC(美国临床遗传药理学实施联盟)、DPWG(荷兰遗传药理学工作组)均有明确说明。CYP1C19等位基因在国人中的权重占比也有显著差异(如下表)。临床医师可以充分采用基因检测手段,评估患者携带的CYP2C19等位基因,根据检测结果识别出可能出现氯吡格雷抵抗的*2和*3 CYP2C19功能缺失等位基因的患者,调整氯吡格雷用药剂量和疗程、换用替格瑞洛等其他抗栓药物、预判PCI术后结果等,达到预前评估、合理选择、精准用药、提高疗效的目的。
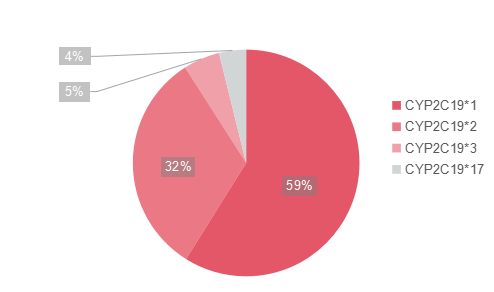
CYP1C19等位基因在国人中的权重占比
二、替格瑞洛的困惑
虽然目前新版指南对于替格瑞洛在直接PCI或溶栓等临床场景中已为ⅠA类推荐,但在我国仍需结合临床实际、国情国体、个体差异而实施具体抗栓策略。因为个体化的差异在中国相当普遍,非统计数据所能涵盖,对老老年、基础疾病多、伴有呼吸困难、心律失常等病例经验更少、数据支持不足,甚至有出现不良反应的报道。这就造成循证医学中整体和局部的矛盾,即指南汇总数据的结论是对宏观全体人员的概括和归纳,但对特殊群体、基因突变型、病情多样性、年龄偏大未在循证医学研究序列的人群等各个情况就需要个体化的分析。临床医师在针对每一个个案病例选择药物时需慎之又慎,指南不会涵盖所有病例,要结合实际、具体分析。至此随着临床应用的增加,替格瑞洛的不良反应逐渐显现出来,主要有心动过缓和房室传导阻滞、出血、呼吸困难、痛风和肾脏损害等。主要的具体表现有如下几点:
01 心动过缓和房室传导阻滞
2020年9月我国NMPA的药物警戒快讯第8期就收录了来自加拿大的替格瑞洛不良反应警告。数据依据来源为加拿大卫生部评估了有心动过缓病史的患者使用替格瑞洛后会发生缓慢性心律失常(心动过缓)恶化的风险(具体数值如下表)。而临床上ACS往往伴有缓慢性心律失常,特别是下壁心肌梗死时常造成双节病变,窦性停搏和房室传导阻滞时有出现,这就增加了使用替格瑞洛出现不良反应的不确定性。
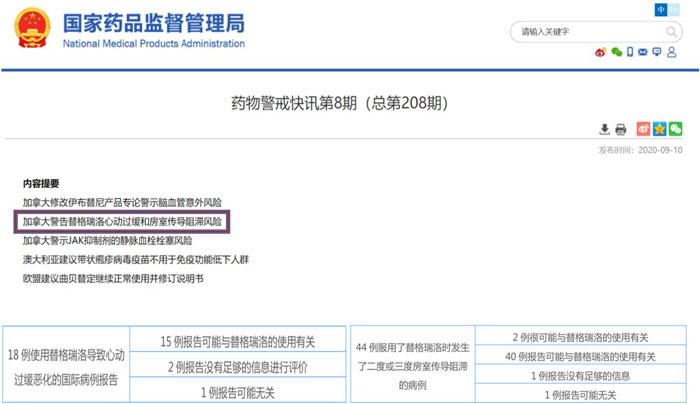
02 出血风险
临床试验研究中,虽然短期替格瑞洛和氯吡格雷的出血发生率相似,但长期应用替格瑞洛的出血风险略高于氯吡格雷,替格瑞洛高达11.6%,其中严重出血占7.9%。
一项基于东亚人群的KAMIR-NIH的研究显示,替格瑞洛在≥75岁患者中的大出血风险明显高于氯吡格雷。所以2018年《急性冠状动脉综合征特殊人群抗血小板治疗中国专家建议》对于年龄≥75岁的ACS患者,建议在阿司匹林基础上选择氯吡格雷作为首选的P2Y12抑制剂。用法为75mg、1次/d,如此次发病前未用此药,建议予负荷量300mg。建议DAPT疗程为12个月,可根据患者缺血与出血风险适当延长或缩短。
03 呼吸困难
多项调查研究均报道,服用替格瑞洛后可能会发生相关的呼吸困难。
在ONSET/OFFSET研究中,使用替格瑞洛治疗的患者出现呼吸困难占24.6%,较氯吡格雷组3.7%的发生率高近7倍。
另一项PLATO研究显示,替格瑞洛组发生静息时呼吸困难、劳力性呼吸困难、阵发性夜间呼吸困难等呼吸困难不良反应的患者约占13.8%;呼吸困难的发生容易导致患者停药,在该试验中替格瑞洛由于出现呼吸困难而停药的比例为0.9%,而氯吡格雷仅0.1%。
GLOBAL-LEADERS 研究探索了 PCI 术后患者降阶治疗的疗效。结果显示,替格瑞洛单药治疗在安全性方面并未表现出显著获益(2.04% vs 2.12%, p = 0.77),反而由于替格瑞洛导致的呼吸困难增加了停药风险。
而临床实际病例中,ACS或脑卒中时常伴有慢性阻塞性肺气肿、肺源性心脏病等基础呼吸系统疾病,这就造成选择替格瑞洛的困惑。
因此,我们应当理性的看待相关结果,在出现更多循证证据之前,临床实际操作层面上,对有基础呼吸系统疾病、慢性心律失常、活动性出血倾向等情况的患者在使用替格瑞洛时,需谨慎评估和分析,合理采取以阿司匹林为基础的双联抗血小板治疗方案。
小结——勿信“万金油”
在罹患ACS并行PCI或溶栓后,阿司匹林联用P2Y12受体拮抗剂是指南推荐的标准疗法。与氯吡格雷相比,替格瑞洛具有更快、更强及更一致的抑制血小板效果,且作为条件限制下的首选方案。但服用替格瑞洛后部分患者可能发生心律不齐、出血及呼吸困难等多种不良反应,且大于75岁的老年人、伴发严重基础疾病等临床病例无大样本统计数据支持,因此我们不能将替格瑞洛当成万金油。对于一些特殊人群我们可以采用基因检测手段,评估氯吡格雷相关CYP2C19等位基因的突变类型,合理选用合适的P2Y12受体拮抗剂是明智的选择。
参考文献:
[1] Park, K. H., et al. (2016). Comparison of short-term clinical outcomes between ticagrelor versus clopidogrel in patients with acute myocardial infarction undergoing successful revascularization; from korea acute myocardial infarction registry-national institute of health. International Journal of Cardiology, 193-200. DOI: 10.1016/j.ijcard.2016.04.044.
[2] (2010). Reduced-function cyp2c19 genotype and risk of adverse clinical outcomes among patients treated with clopidogrel predominantly for pci:content. JAMA, 304(16), 1821-1830. DOI: 10.1001/jama.2010.1543.
[3] 中华医学会心血管病学分会, & 中华心血管病杂志编辑委员会. (2019). 急性st段抬高型心肌梗死诊断和治疗指南(2019). 中华心血管病杂志, 47(10), 766-783.DOI: 10.3760/cma.j.issn.0253-3758.2019.10.003.
[4] 王斌. (2018). 稳定性冠心病诊断与治疗指南. 中华心血管病杂志(09), 680-694. DOI: CNKI:SUN:ZHXX.0.2018-09-006.
[5] 韩雅玲. (2016). 替格瑞洛临床应用中国专家共识. 临床军医杂志. DOI: CNKI:SUN:JYGZ.0.2016-05-002.
[6] Jneid, H., et al. (2017). 2017 aha/acc clinical performance and quality measures for adults with st-elevation and non–st-elevation myocardial infarction. Journal of the American College of Cardiology, 70(16), 2048. DOI: 10.1016/j.jacc.2017.06.032.
[7] Marco, V., et al. (2018). 2017 esc focused update on dual antiplatelet therapy in coronary artery disease developed in collaboration with eacts. European Heart Journal(3), e1. DOI: 10.1093/eurheartj/ehx419.
[8] 中国药师协会. (2019). 急性ST段抬高型心肌梗死溶栓治疗的合理用药指南(第2版). 中国医学前沿杂志(电子版), 11(01), 40-65. DOI: CNKI:SUN:YXQY.0.2019-01-008.







