PIK3CA被写进乳腺癌NCCN指南,你们的报告更新了吗?
2019年7月2日,NCCN发布了乳腺癌指南2019 V2版,较2019 V1版指南中新增了PIK3CA基因突变检测以及针对PIK3CA基因突变的治疗方案——氟维司群联合特异性PI3K抑制剂Alpelisib。
而FDA已于5月24日批准诺华公司(Novartis)的PI3K抑制剂Alpelisib(Piqray)上市,可与内分泌疗法氟维司群联用,用于治疗接受过内分泌疗法后疾病进展、携带PIK3CA基因突变、HR+/HER2-晚期或转移性绝经后妇女和男性乳腺癌患者,值得一提的是这是首款应用于实体瘤的PI3K抑制剂。
仅过去一个月时间,该疗法就被纳入NCCN指南,这标志着乳腺癌靶向治疗进程在加快。下面为大家具体介绍本次NCCN乳腺癌指南更新内容中关于PIK3CA的详细信息。
01 指南重要更新
-
PIK3CA基因检测:
HR+/HER2-的乳腺癌患者如果考虑使用Alpelisib,可以进行组织或血液的PIK3CA基因检测;可以对肿瘤组织或外周血循环肿瘤DNA(ctDNA)进行PIK3CA突变检测,如果液体活检阴性,推荐进行肿瘤组织检测[1];
-
PIK3CA突变阳性治疗方案:对PIK3CA基因突变且HER2阴性的绝经后乳腺癌患者,首选 Fulvestrant(氟维司群)+ Alpelisib 联合治疗方案(1类证据)[1]。
指南中关于PIK3CA的更新主要集中于PIK3CA基因的检测以及后续的治疗方案。需要指出的是在批准该疗法的同时,FDA还批准了其伴随诊断产品——Qiagen的 Therascreen®PIK3CA RGQ PCR Kit,用以检测组织和/或液体活检中的PIK3CA突变,来筛选获益人群[2] 。
02 PI3K抑制剂Alpelisib疗法获批的临床试验
Alpelisib能够获批主要是基于SOLAR-1的研究结果,对入组的572例PIK3CA基因突变(或未突变)的HR+/HER2-晚期或转移性乳腺癌患者中分为两组随机试验。
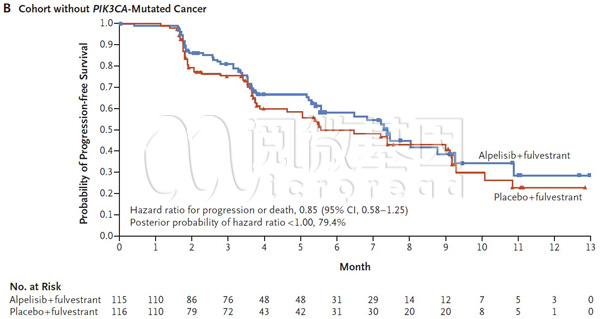
主要终点分析显示,在PIK3CA突变患者中,Alpelisib+氟维司群治疗对比单独接受氟维司群治疗的中位无进展生存期(mPFS)分别为11.0个月vs 5.7个月,几乎翻了一倍,在总体缓解率(ORR)方面也增加了一倍以上(35.7% vs 16.2%)!而在PIK3CA突变阴性的患者中,mPFS 7.4个月 vs 5.6个月,无显著差异[3]。
PIK3CA突变患者中Alpelisib联合氟维司群组与氟维司群单药组PFS对比
PIK3CA突变阴性患者中Alpelisib联合氟维司群组与氟维司群单药组PFS对比
HR+乳腺癌约占乳腺癌发病病例的75%,而PIK3CA是HR+乳腺癌最常见的突变基因,占到40%左右[4]。PIK3CA基因突变与疾病进展、内分泌抵抗以及总体预后不良有关。Alpelisib针对PIK3CA基因突变,有助于克服HR+/HER2-晚期乳腺癌的内分泌抵抗。
03 乳腺癌精准治疗
近年来乳腺癌发病率逐年递增,已成为威胁中国女性生命健康的第一大恶性肿瘤。虽然乳腺癌发病率越来越高,但死亡率受到了很好的控制。从2000年到2011年中国乳腺癌每年发病率增长速度平均是3.9%,死亡率的年增长相对较缓,只有1.1%[5],这与乳腺癌的精准治疗密不可分。
乳腺癌是较早开展靶向治疗的癌种之一。自HER2靶向药物曲妥珠单抗问世以来,乳腺癌的靶向治疗家族成员不断增加,比如拉帕替尼、CDK4/6抑制剂、PARP抑制剂奥拉帕利等等,这些药物给乳腺癌患者的生存带来了巨大改善,为广大乳腺癌患者带来了希望。
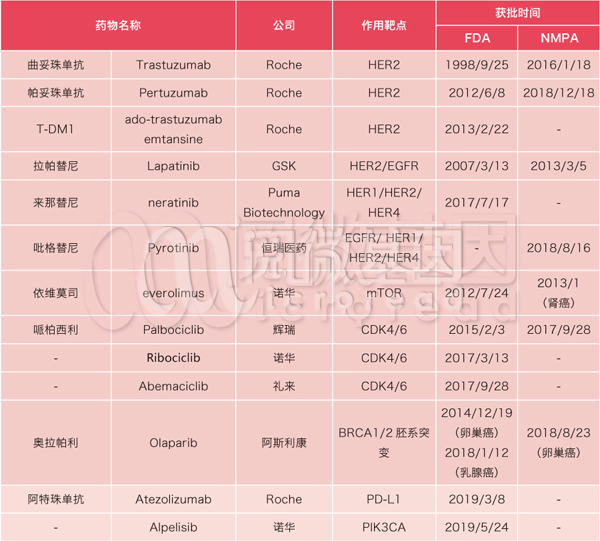
乳腺癌常见靶向及免疫治疗药物
*数据来源:FDA、医药魔方、中信建投证券研究发展部
如上表所示,2019年上半年除PIK3CA抑制剂Alpelisib获批外,还有罗氏公司的PD-L1抑制剂阿特珠单抗(Atezolizumab)。阿特珠单抗联合化疗用于一线治疗无法切除的局部晚期或转移性PD-L1阳性的三阴性乳腺癌(TNBC)患者,这是首个获批的乳腺癌免疫疗法,标志着乳腺癌的临床治疗自此进入免疫治疗时代[6-7]。
Alpelisib和阿特珠单抗这两种药物被批准用于转移性乳腺癌患者的治疗,并且明确了患者需具有相应的分子靶标才可以使用药物,无疑加速了乳腺癌精准治疗的进程。
从乳腺癌今年两大新药的获批以及相应分子生物标志物的发现,反映出肿瘤精准医疗领域进程的加快,更加准确、个体化的肿瘤治疗方案无疑给肿瘤患者的临床治疗带来新的希望,我们也期待免疫治疗领域涌现越来越多的适合不同患者应用的治疗方案。
参考文献:
1. Breast Cancer NCCN Clinical Practice Guildliness In Oncology (2019 V2)
2. https://www.fda.gov/news-events/press-announcements/fda-approves-first-pi3k-inhibitor-breast-cancer
3. André F et al. (2019). Alpelisib for PIK3CA-Mutated, Hormone Receptor–Positive Advanced Breast Cancer. New England Journal of Medicine.
DOI: 10.1056/NEJMoa1813904
4. Juric D, et al. (2019). Alpelisib Plus Fulvestrant in PIK3CA-Altered and PIK3CA-Wild-Type Estrogen Receptor–Positive Advanced Breast Cancer: A Phase 1b Clinical Trial. JAMA oncology.
DOI: 10.1001/jamaoncol.2018.4475
5. Chen W, et al. (2019). Cancer statistics in China, 2015. CA Cancer J Clin.
DOI: 10.3322/caac.21338
6. FDAGrants Genentech’s Tecentriq in Combination With Abraxane Accelerated Approvalfor People With PD-L1-Positive, Metastatic Triple-Negative Breast Cancer.
7. Schmid P, et al. (2018). Atezolizumab and Nab-Paclitaxel in Advanced Triple-Negative Breast Cancer. N Engl J Med.
DOI: 10.1056/NEJMoa1809615.