2016年生命科学领域5大争议事件:韩春雨、血液女神在列
导读
2016年生命科学领域获得了多项突破,也发生了一些颇受争议的的事件,在回顾过去的这一年中生命科学领域事件的同时,有一群默默无闻的人也在不懈的努力,成就了大大小小的突破,阅微基因也是其中之一。
阅微基因一贯坚持以技术创新为基础,依托专业的研发团队和科技平台,为生命科学研究提供技术服务,加速研究者的实验;研发生产DNA建库试剂盒、亲缘鉴定试剂盒、案件DNA检测试剂盒、基因检测试剂盒,特别值得一提的是新研发成功的29Y鉴定试剂盒及鉴定软件为公安系统的家系排查工作带来了大大的便利性。
2017,我们将继续追踪现代分子医学及基因检测的发展趋势,研发储备前瞻性的基因检测、临床和法医鉴定试剂以及临床检测自动化系统,以创新谋发展,通过强大的技术力量、高素质的研发团队、卓越的产品性能、一流的售前售后服务以及严谨科学的现代化企业管理制度,力图成为国内基因检测行业领跑者。
2016年,生命科学领域获得了多项突破。前几日,Nature和Science网站相继评出了2016年产生重大影响的科学事件,其中包括CRISPR人体临床试验、孔纳米测序、寨卡病毒、三亲婴儿、杀死老细胞永葆青春、计算机设计人工蛋白以及实验室制造小鼠卵子。2016年,生命科学领域也发生了一些受到争议的事件。近日,TheScientist网站对这些事件进行了汇总。这些争议事件涉及了技术专利、论文造假、伦理与道德......
1、学术不端的纠纷

PubPeer是一个2012年上线的允许同行在论文出版后发表匿名评论的平台。Wayne州立大学的癌症研究员FazlulSarkar是500多篇论文的署名作者,2014年PubPeer有匿名评论称Sarkar超过50篇存在问题,比如描绘不同实验的图像之间非常相似,而这些评论严重影响了他的仕途。在2014年,Sarkar首次对同行评审网站PubPeer匿名评论者提出诉讼。
2016年初,FazlulSarkar发誓要继续利用法律手段来打击这位匿名评论者。1月份,密歇根州法庭下令要求PubPeer向Sarkar的法律团队公开匿名评论者。PubPeer对此提出了上诉。前美国国家癌症研究所主任HaroldVarmus、科学杂志前主编BruceAlberts、科技巨头谷歌和Twitter提交了法庭之友对PubPeer和匿名评论者表示支持。
今年10月份,听证会透露了一些信息:PubPeer曾试图停止收集匿名评论者的IP地址,以避免面对类似的法律诉讼案件。去年Wayne州立大学对Sarkar开展内部调查,调查报告显示,在过去的几年里,Sarkar存在科研不端行为。
尽管经历了波折,上诉法庭裁定PubPeer的匿名评论规则保持不变,因为匿名评论受美国宪法第一修正案所保护。这则曲折的纠纷下一步会发生什么?目前尚未清楚,但本月早些时候,Sarkar的律师表示尚未确定是否决定向密歇根州最高法院提出上诉......
2、韩春雨的重复试验

今年,有一篇论文受到了国内外的争议。六个月前,韩春雨报道了一种称为NgAgo的酶可以用于编辑哺乳动物基因,而且这一技术要比目前流行的CRISPR-Cas9基因编辑技术更为精确和应用广泛。但是在文章公布后,围绕着NgAgo基因编辑技术,科学界议论纷纷。
目前,距离韩春雨课题组在《自然-生物技术》上发表关于基因编辑技术NgAgo的论文,已经过去7个多月,全球尚无一家实验室宣布能重复NgAgo实验。
韩春雨的重复试验成为了国际国内学者关注的焦点。今年11月份,《自然-生物技术》发表了韩国首尔大学、德国弗莱堡大学和美国梅奥研究生院等研究机构10位科学家表示使用NgAgo无法检测到基因组编辑效果的来信。《自然-生物技术》表示,调查将于2017年1月底之前完成,届时将公布最新进展。
3、CRISPR的专利纠纷

2016年伊始,美国专利和商标局(USPTO)开始确定谁将拥有CRISPR/Cas9的专利权,CRISPR/Cas9的专利之战也开始趋于白热化。
CRISPR/Cas是在大多数细菌和古细菌中发现的一种天然免疫系统,可用来对抗入侵的病毒及外源DNA。2012年,加州大学伯克利分校生物学家JenniferDoudna和另一CRISPR先驱EmmanuelleCharpentier(现在就职于德国柏林马克斯普朗克研究所和默奥大学)领导的研究小组发表的一篇关键文章中揭示了天然免疫系统是如何变成编辑工具的。 接下来,科学家需要证明的是这种充满魔法的编辑工具能否运用到人类细胞的基因组上。2013年1月,哈佛大学的GeorgeChurch实验室和Broad研究所的张锋发表文章证实了上述问题的答案是肯定的。JenniferDoudna在几周后,也发表了她自己的结果。2013年10月,张峰所在的研究所提出了CRISPR-Cas9技术专利的加急申请,该专利申请在2014年4月被通过了,张峰也被授予其他相关技术的专利。而早在2013年3月由JenniferDoudna和EmmanuelleCharpentier提出的专利申请仍在审查之中。
2016年1月11日,美国专利商标局同意了开始审核“CRISPR-Cas9专利”。该专利究竟会花落谁家,可能会决定价值数百万美元专利被哪个研究机构拥有。这也可能影响到谁会被允许使用该技术,以及在何种条件下使用CRISPR/Cas9基因编辑系统。
决定谁将在这场专利纠纷中获胜的关键因素回归到了单一的问题上:在Doudna及其团队确定信号通路的组成之后,CRISPR是否明显被应用于真核生物中?或者说这些应用是否需要更多的创新?
获得首个CRISPR专利的Broad研究所认为,张峰的创新是CRISPR在真核生物中得到应用的关键,加州大学伯克利分校申请的专利属于明显的干扰;不过Doudna及其同事的前期工作以及CRISPR应用于体外及原核生物中的专利申请应获得有价值的知识产权。
英国HGFLimited的高级专利律师CatherineCoombes指出,领域内外的研究员应该对这类争端提高警惕,采取适当的预防措施,以避免工作中遭遇麻烦的知识产权纠纷。
4、首例三亲婴儿的诞生
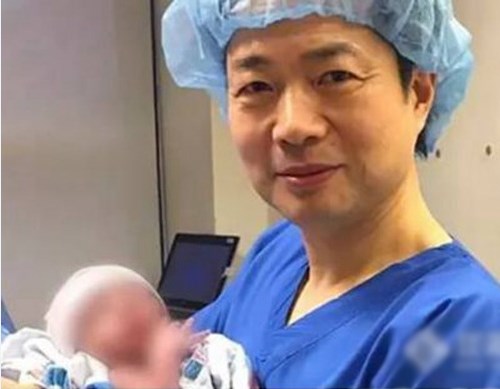
全球首例三亲婴儿已于今年4月份在墨西哥诞生。纽约新希望生殖医学中心的华人医学博士JohnZhang采用了线粒体替代疗法、PGS和NGS技术,成功帮助线粒体基因缺陷女子产下了健康后代。首例三亲婴儿的诞生也成为了2016年度最受争议的话题之一。
对于携带线粒体疾病的女性而言,线粒体替代疗法是帮助她们生育健康宝宝的强有力技术。近年来这项技术也不断获得突破。最近Nature上的一项研究也展示了如何减少有缺陷的线粒体随细胞核进入供体卵子的风险。其他研究也揭示了供体卵子和母亲卵子线粒体DNA单倍型匹配的重要性。
今年,关于三亲婴儿技术的监管也迎来了热议。目前美国禁止该技术,而12月16日,英国人类受精与胚胎管理局对该技术开了绿灯。由于这项技术需要在实验室以及诊所中进行多种测试,因而它有可能继续受到世界各地监管机构的关注。
来自哥伦比亚大学内科与外科学院的JohnLoike和NancyReame在一篇科学评述中表示,“线粒体替代疗法有望成为线粒体疾病女性生育健康宝宝的有效方法,它不应该因社会或道德的复杂性而被禁止。鉴于潜在地永久性改变DNA,这项技术不应该被视为与传统的器官捐赠等同,而应该与其他生殖系统干预的管理一样,如捐赠卵子或精子,目前这方面的监管已经到位了。将这些作为监管框架,各国政府和科学界应该投入时间和金钱,使技术能被广泛使用。”
今年7月份,经过联邦政府的调查(包括刑事调查),Theranos的创始人兼首席执行官ElizabethHolmes被禁止在未来两年内运营任何血液检测实验室,同时Theranos的加州实验室也被关闭——那里正是该公司从事试验性“一滴血”验血技术的地方。
8月份,Elizabeth在美国临床化学协会发表了演讲,这次她并未针对公司现有的技术和问题,而是展示了对新设备的想法,这个设备也被称为miniLab。不过当时听众对她这场演讲的印象并不深刻。
然而,Theranos在10月份宣布将公司的方向从血液检测转移至科研,Elizabeth在给股东的信件中表示接下来要把注意力放在miniLab平台上。同在10月份,《华尔街日报》报道了患者被Theranos血液检测结果误导的案例,后来投资者也表示他们被Theranos公司误导,同时美国最大的连锁药店Walgreens控告Theranos违反合同约定,并索赔1.4亿美元。






